안녕하세요!!~~ 슈뢰딩거 입니다! 화2 정리 첫번째 글이에요! 화 2 내용이 드럽게 많고 이해하기도 힘들 뿐더러 외우기도 힘들기 때문에 제게 도움이 도움이 되면서 여러분들 또한 도움이 되는 방법으로 노트 필기가 아닌 블로그 작성을 선택하게 되었어요! 여러분들이 제 블로그의 방문자 이기도 하지만 저 또한 이 글을 읽기 때문에 :) 좀 더 읽기 편한 ~하요체(비격식체)를 사용할께요~~ ㅎㅎ 제 글을 읽어주시는 모든 분들께 감사드립니다!
일단 이 글의 난이도는 화 1을 모두 마치고 난 분이 가장 이해하기 쉬우실 꺼에요! 왜냐하면 저도 지금 처음으로 화2를 배우고 있고, 그래서 제가 쓰는 화2의 개념은 심도있게 다룰꺼지만(심화내용) 처음 화2를 보시더라도 이해할 수 있도록 작성하도록 노력할껍니다!
또한 이 강의의 특징이라고 하면 부연설명도 (하이탑처럼) 많지만 정말 중요한 부분(수식 제외)은 하이라이트를 쳐서 2~3번 읽으시는 분들을 위해 가독성을 높일겁니다!
하지만 처음 읽는 분께서는 꼭 정독해주시기 바랍니다!
한가지 더 중요한 부분은 수식 기호 설명입니다! 저는 개인적으로 수식에 들어가는 기호의 뜻을 잘 외우지 못하기 때문에ㅠ 써놓도록 하겠습니다!(하지만 귀차니즘 때문에 설명에 들어가는 기호와 수식에 들어가는 기호는 다를 수 있습니다)
목차
1. 분자간 힘
(1) 분자간 인력의 중요성
(2) 쌍극자-쌍극자 힘
(3) 분산력
(4) 수소결합
(5) 쌍극자-유발쌍극자 힘
(6) 이온-쌍극자 힘
(7) 이온-유발쌍극자 힘
1. 분자간 인력의 중요성
인력의 중요성 이라기 보다는 분자간 인력이 달라지면 무엇이 변하는가 정도로 해석해 주시면 될 것 같습니다.
1. 녹는점. 끓는점이 변화
분자간 인력이 셀수록 끓는점은 올라가게 됩니다. 가열곡선의 y값이 전체적으로 증가한다는 뜻이지요.
2.
2. 쌍극자-쌍극자 힘
이 인력이 작용하는 원리를 알기 위해선 먼저 편극에 대한 이해가 필요합니다. 편극이란, 분자 안에서 각각 원자의 분자량이 불균형을 이룰 때 발생합니다.
예를 들어, 물 분자가 있다고 가정을 하면 H의 분자량은 1인데 비해 O의 분자량은 16에 달합니다.
그렇다면 전자는 핵과의 약력에 의해 핵 주위를 돌고 있는건데, 옆에서 더 쎈 약력을 가진 핵이 등장한다면 전자는 더 무거운 핵으로 끌려가게 되고, 그렇게 되면 H는 O에 비해 상대적으로 이온화가 되어 +극을 가지게 되는 것이죠.
반대로, O는 전자가 원래에 비해 많아졌으니 상대적으로 -극을 가지게 됩니다. 이게 편극현상이며, 그림으로 표현하면 아래와 같고, 극 앞에 붙이는 기호를 '델타' 라고 읽습니다.
http://study.zum.com/book/14980
|
쌍극자-쌍극자 힘은 쌍극자 모멘트를 기초로 하여 생기는 인력 입니다.
그럼 쌍극자 모멘트에 대해 설명해 드리겠습니다. 쌍극자 모멘트란, 극성 분자(대칭이 아닌 분자)에서 생기는 편극 현상 모두의 합력으로, (+) 전하에서 (-) 전하로 향하는 갖는 벡터량 입니다. 예를 하나 들어보겠습니다. 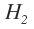 의 경우 입니다.
의 경우 입니다.
이 분자는 서로 끌어당기는 힘은 있지만 알짜힘이 0이므로 쌍극자 모멘트는 0입니다.
하지만 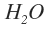 의 경우, 상대적으로 무거운 산소가 두개의 수소를 끌어당깁니다. 편극현상이 일어나게 됩니다. 이경우, 쌍극자 모멘트는 H에서 O를 향하는 방향의 두 힘을 합친 벡터량이 됩니다.
의 경우, 상대적으로 무거운 산소가 두개의 수소를 끌어당깁니다. 편극현상이 일어나게 됩니다. 이경우, 쌍극자 모멘트는 H에서 O를 향하는 방향의 두 힘을 합친 벡터량이 됩니다.
쌍극자와 유발쌍극자를 각각 극성분자, 무극성 분자라고 지칭하기도 하죠. 그래서, 쌍극자-쌍극자 힘은 극성 분자 사이에 작용하는 인력 입니다.
자 그럼 쌍극자-쌍극자 힘이란 무엇일까요?
모든 극성 분자는 편극현상이 나타납니다. 만약 같은 극성 분자 몇개를 가져다 놓는다면, 이러한 그림이 생겨납니다.
http://study.zum.com/book/14605
|
(물분자를 예로 들지 않은 것은 쌍극자-쌍극자 힘도 존재하지만 수소결합이 훨씬 강하게 작용하기 때문입니다)
델타 +의 H원자가 다른 분자의 Cl원자와 인력이 작용하네요! 델타 -의 Cl원자도 다른 H원자를 끌어당기고 있습니다.
이를 쌍극자-쌍극자 힘이라고 합니다.
쌍극자-쌍극자 힘과 쌍극자 모멘트의 차이는 쌍극자 모멘트는 분자 안에서 일어나는 인력인데 반해 쌍극자-쌍극자 힘은 분자 사이에서 일어나게 됩니다. 비유를 하자면, 쌍극자 모멘트는 자석의 원리 이고, 쌍극자-쌍극자 힘은 자석 사이에 일어나게 되는 인력 입니다.
3. 분산력
분산력이란 어느 분자나 분자사이에 작용하는 인력입니다. 무극성 분자의 경우, 수소결합이나 쌍극자-쌍극자 힘과 같은 인력이 작용하지 않습니다. 이유는 아시다시피 두 힘은 특정 분자 사이에 작용하는 인력이기 때문입니다. 하지만 분산력은 만약 그 분자가 극성이라도, 무극성 이라도, 수소결합이더라도 존재하게 됩니다.
분산력은 순간쌍극자-유발쌍극자 인력에 의해 생깁니다.
순간 쌍극자는 무극성 분자의 전자들이 확률에 의해(전자들의 위치가 확률에 의해 결정되므로) 한쪽에 몰려가 짧은 시간동안 쌍극자 모멘트를 갖게 되는 것 입니다.
그런데 이때, 같은 종류의 다른 분자가 옵니다. 이 경우 정전기 유도현상에 의해 전 분자에 의해 후 분자의 쌍극자가 유발되므로 유발쌍극자 라고 합니다.
한줄로 정리하자면, 우연으로 생긴 쌍극자와 그로 인해 생기는 다른 분자들의 쌍극자가 분산력 이라는 것 입니다.
4. 수소결합
수소결합은 수소 원자와 F, O, N 원자가 공유결합을 형성(H-(F, O, N))할때, 이 분자와 다른 같은 종류의 분자사이의 인력이 수소결합 입니다. 
이때 저 중간의 점선은 수소결합을 나타내는 결합선 입니다.
수소결합의 세기를 결정하는 요인은 수소에 결합된 원자의 전기음성도 크기입니다.
왜냐하면, 만약 수소와 질소가 결합했다고 칩시다. 그러면 3개의 수소는
모두 전자를 약간씩 빼앗기게 되며, 이때 델타 +가 됩니다.
반대로 질소는 델타 -가 됩니다. 뭐 여기까지는 다 예상 하셨겠지만…
수소의 배신이 일어나요. 전자를 거의 뺏겨버린 양성자 하나가 이제 다른 분자의 비공유 전자쌍(F, O, N)을 찾으러 가게 되고, 그러면서 저 점선이 생기게 됩니다. 그렇다면, 전기음성도의 크기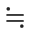 수소의 원자핵 노출 정도
수소의 원자핵 노출 정도 수소 결합의 세기
수소 결합의 세기
가 되죠.
수소 결합도 인력중 하나이기 때문에 수소결합 세기가 세지면 끓는점도 높아집니다.
5. 쌍극자-유발쌍극자 힘
대충 이해는 가실껍니다. 극성 분자와 무극성 분자에 작용하는 힘이죠.
예를 들어, 무극성 분자는 바깥에 전자들이 고르게 배치되어 있습니다. 하지만 극성 분자가 다가오게 되면, 다가오는 쪽이 델타 - 를 띌 경우 무극성 분자에서는 전자들이 한쪽으로 몰리게 됩니다. 마치 자석이 같은 극을 싫어하듯이요.
그렇게 되면 무극성 분자는 극성분자에 의해 덩달아 편극이 됩니다. 극성 분자에 의해 생기게 된 무극성 분자의 유발 쌍극자와 쌍극자 사이의 힘을 쌍극자-유발쌍극자 힘 이라고 합니다.
6. 이온-쌍극자 힘
원래 +나 -를 띄고 있던 이온이 델타+나 델타 -를 띄고 있는 극성분자에게 작용하는 힘 입니다. 강한 힘을 가지며, 이러한 현상의 예로는 수화 현상이 있습니다.
7. 이온-유발쌍극자 힘
이온과 이온에 의해 유발된 쌍극자(무극성 분자)와의 인력 입니다. 약해요.
감사합니다. Copyright.2017.류관형.All rights reserved
궁금한점 있으시면 댓글로 달아주세요.

야이시발놈아 이유가 부족해
답글삭제